Kalor adalah Energi panas yang mengalir dari zat bersuhu tinggi ke zat bersuhu rendah. Satuan kalor adalah kalori (kal) dan untuk satuan yang lebih besar digunakan kilo kalori (kkal). 1kilo kalori (kkal) sama dengan 1000 kalori (kal). Karena kalor merupakan bentuk energi, kalor memiliki satuan dalam SI, joule (J). Melalui pengamatan James Presscott Joule, menyimpulkan bahwa 1 kalori sama dengan 4,184 joule atau dibulatkan 4,2 Joule.
Kalor dapat berpindah dari benda yang bersuhu tinggi ke benda yang suhunya lebih rendah. Ada tiga cara perpindahan kalor, yaitu secara konduksi, konveksi, dan radiasi.
Besarnya kalor suatu zat dipengaruhi oleh perubahan suhu, massa zat, dan jenis zat. Beberapa persamaan atau rumus kalor antara lain sebagai berikut :
Diketahui :
m = 500 gram
c = 0.5 kal/gr⁰C
ΔT = -2 ⁰C – (-12⁰C) = 10⁰C
Ditanya :
Q ?
Jawab :
Q = m.c.ΔT
Q = (500).(0.5).(10)
Q = 2500 kalori
Ingat 1 kalori = 4.2 joule maka,
2500 (4.2) = 10.500 Joule
Jadi kalor yang diperlukan utuk memanaskan es tersebut sebesar 10.500 Joule.
2. Berapa kalor yang dibutuhkan untuk memanaskan 1 kg air yang bersuhu 20⁰C menjadi 100⁰C jika diketahui kalor jenis air 1000 J/kg⁰C ?
Diketahui :
m = 1 kg
c = 1000 J/kg⁰C
ΔT = 100⁰C - 20⁰C = 80⁰C
Ditanya :
Q ?
Jawab :
Q = m. c ΔT
Q = 1. 1000. 80
Q = 80.000 J
Jadi kalor yang
diperlukan untuk memanaskan air tersebut sebesar 80.000J atau 80KJ.
Bonus Tebak Tebakan :
Becak apa yang tidak bisa di cat ?
Becak hilang
Kalor dapat berpindah dari benda yang bersuhu tinggi ke benda yang suhunya lebih rendah. Ada tiga cara perpindahan kalor, yaitu secara konduksi, konveksi, dan radiasi.
- Konduksi adalah proses perpindahan kalor yang terjadi tanpa disertai dengan perpindahan partikel partikel dalam zat itu.
- Konveksi adalah perpindahan kalor yang disertai dengan perpindahan partikel partikel zat tersebut yang disebabkan oleh perbedaan massa jenis zat
- Radiasi adalah perpindahan kalor tanpa adanya zat perantara.
Besarnya kalor suatu zat dipengaruhi oleh perubahan suhu, massa zat, dan jenis zat. Beberapa persamaan atau rumus kalor antara lain sebagai berikut :
Jika dua benda memiliki suhu yang berbeda kemudian dicampur, pada benda tersebut akan terjadi proses melepas dan menerima kalor. Dalam mekanisme penyerapan dan pelepasan kalor oleh suatu benda ini berlaku hukum kekekalan energi, dimana "kalor yang dilepaskan akan sama dengan kalor yang dierap". Pernyataan ini dikemukakan oleh Joseph Black dan dikenal sebagai Asas Black. Secaramatematis, Asas Black dapat dituliskan sebagai berikut :
Contoh Soal :
1. Tentukan banyaknya kalor yang diperlukan untuk memanaskan 500gram es yang bersuhu - 12⁰C menjadi - 2⁰C. Nyatakan dalam satuan joule jika diketahui kalor jenis es 0.5 kalori/gr⁰C !
Diketahui :
m = 500 gram
c = 0.5 kal/gr⁰C
ΔT = -2 ⁰C – (-12⁰C) = 10⁰C
Ditanya :
Q ?
Jawab :
Q = m.c.ΔT
Q = (500).(0.5).(10)
Q = 2500 kalori
Ingat 1 kalori = 4.2 joule maka,
2500 (4.2) = 10.500 Joule
Jadi kalor yang diperlukan utuk memanaskan es tersebut sebesar 10.500 Joule.
2. Berapa kalor yang dibutuhkan untuk memanaskan 1 kg air yang bersuhu 20⁰C menjadi 100⁰C jika diketahui kalor jenis air 1000 J/kg⁰C ?
Diketahui :
m = 1 kg
c = 1000 J/kg⁰C
ΔT = 100⁰C - 20⁰C = 80⁰C
Ditanya :
Q ?
Jawab :
Q = m. c ΔT
Q = 1. 1000. 80
Q = 80.000 J
Jadi kalor yang
diperlukan untuk memanaskan air tersebut sebesar 80.000J atau 80KJ.
Bonus Tebak Tebakan :
Becak apa yang tidak bisa di cat ?
Becak hilang

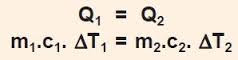
No comments:
Post a Comment